
可塑剤の安全性について
- トップページ
- 可塑剤の安全性について
 可塑剤工業会
可塑剤工業会
可塑剤工業会は科学的な根拠に基づき可塑剤の安全性を主張してきました。可塑剤の安全性について可塑剤工業会の見解を以下にお示しします。
毒性とは、化学物質等による生物に悪影響を与える性質で、一般毒性1)と特殊毒性に分けられます。一般毒性は、血液検査、尿検査、病理組織学的検査等の一般的な方法で観察できる毒性を言い、急性毒性と慢性毒性に分けられます。本章では、代表的な急性毒性について、概要と主要可塑剤の実データをもとにした安全性に対する見解を記します。
また、特殊毒性は、CMR(発がん性 Carcinogenic,変異原性 Mutagenic,生殖毒性Reprotoxic)や催奇形性などの特殊な観察法によって評価される毒性で、詳細は別章を参照ください。
(1)急性毒性
1回の投与(ばく露)または短期間の複数回投与によって短期間(終日~2週間程度)に生じる毒性で、同量投与された個体のうち半数が死に至る用量 LD50 (半数致死用量)、または濃度 LC50 (吸入毒性の場合、半数致死濃度)で表します。単位としては LD50(用量)では mg/kg(体重1kg当りの投与 mg)、LC50(濃度)では mg/L(1リットル中の吸入ミスト中濃度)等を用います。毒物・劇物は毒物及び劇物取締法にてこの LD50 を目安に指定されています。
ここで、LD50(経口)について、主要可塑剤の可塑剤工業会(JPIA)発行 SDS2)記載データと GHS 分類結果を表1に記載します。全ての可塑剤の GHS 分類は、「区分に該当しないとなっております。また、砂糖の LD50 は 8-10 (mg/kg)、食塩は 8-12 (mg/kg)であることをあわせて考えると、可塑剤の急性毒性は問題ないレベルであると考えられます。
表1.主要可塑剤のLD50(経⼝)と可塑剤⼯業会のGHS分類結果
| DBP | DOP | DINP | DIDP | DOA | DINA | TOTM | TCP | ||
| LD50経⼝ (g/kg)或いは(ml/kg) |
5.3-8 | 26-34 | ≧10 | 22.5- 64 |
73.9- 250 |
≧5 | ≧20 | 31 | |
| JPIA GHS 分類 |
区分に 該当しない |
〇 | 〇 | 〇 | 〇 | 〇 | 〇 | 〇 | 〇 |
| 分類できない | |||||||||
1) http://kinkiagri.or.jp/library/shoku_an_an/dokusei.htm
2) http://www.kasozai.gr.jp/sds/
1980年代はじめに極めて高濃度のDEHPをラットに投与すると肝臓に腫瘍を引き起こすことが報告されましたが、その後の研究で肝腫瘍は、PPAR-α(α型ペルオキシソーム増殖剤活性化受容体(Peroxisome Proliferator-Activated Receptor-α))を介したげっ歯類に特有のメカニズム(メカニズム1)で起きることが明らかになりました。これを受けIARC(国際がん研究機関(International Agency for Research on Cancer))は2000年にヒトへの発がん性はないとして従来の「グループ2B」(ヒトに対して発がん性がある可能性がある)を「グループ3」(ヒトに対する発がん性について分類できない)に変更しました。
更に、IARCは2011年2月の会議で再びDEHPを「グループ2B」に戻すと決定しました。げっ歯類の発がん性が必ずしもげっ歯類固有のPPAR-αを介したメカニズムばかりではなく、他のメカニズム(メカニズム2)によっても生じ得ることが報告され、そのメカニズム2がヒトにも当てはまるか否か2011年の段階では判断ができなかったからです。げっ歯類におけるそのような発がん性のメカニズム(メカニズム2)がヒトにも適用できるかどうかを調査する研究が現在も継続されています。なお、他の可塑剤はIARCでは発がん性評価による分類はなされていないようです。
2023年12月時点でのIARCの分類を幾つかの物質について下に示しておきます。

生殖毒性は化学物質にばく露された「雌雄の成体の生殖機能及び受精能力に対し悪影響を及ぼす性質及び子の発生に対し悪影響を及ぼす性質」と定義されています1)。
化学物質による悪影響を及ぼす性質には雌雄生殖器官の変化、生殖可能年齢の開始時期、配偶子の生成及び移動、生殖周期の正常性、性的行動、受精能/受胎能、分娩、妊娠の予後に対する悪影響、生殖機能の早期老化、又はその他の正常な生殖機能からの変化等が含まれます。
可塑剤工業会では、フタル酸エステルの安全性について科学的な検証を進めています。研究に使用される実験動物であるげっ歯類と我々が属する霊長類では、「生物学上の種の違い」による毒性の発現に差異があるのでないかという視点に立って検証を行っています。
直近では、霊長類であるヒトとカニクイザル、及びラットに対して、それぞれの肝細胞を用いてMEHPとMINPのin vitroでの代謝実験を実施しました(MEHPはジエステルであるDEHPのモノエステルであり、MINPも同様にDINPのモノエステルです)。その実験結果をごく簡単に以下ご説明します。げっ歯類と霊長類の肝細胞におけるフタル酸エステルの代謝のプロフィールは異なり、霊長類(ヒトとカニクイザル)においては、げっ歯類(ラット)より極めて速くモノエステルをグルクロン酸で抱合し、肝細胞の中で代謝物を無毒化していることが明らかにされました。これまでの、マーモセット、ヒト、キメラマウスを対象とした一連の実験結果と共に、このin vitroの実験結果も首尾一貫した種差が認められたことから、可塑剤工業会はDEHPの生殖毒性はヒトを含む霊長類には発現し難いとの考えをこれからも堅持、主張してゆきたいと考えています。また、これまでに公表された各国の評価書においても種差のあることが認められています。
参考
1)政府向けGHS分類ガイダンス(令和5年度改訂版(Ver2.2))
https://www.meti.go.jp/policy/chemical_management/int/files/ghs/ghs_auto_classification_tool/ghs_classification_guidance_for_government_2024.pdf
化学物質のばく露により遺伝子に異常が生じるか否かを調べるのが、変異原性試験です。最近では、変異原性試験においても、化学物質の構造の類似性から、既知の化学物質のデータを基にしたモデル計算で、未知の化学物質の変異原性がたちどころに出るシリコサイエンスが流行りかけています。
DEHPを例にとってお話ししましょう。DEHPは、遺伝子関連の種々のアッセーで集中的に試験されてきましたが、その結果得られたエビデンスからDEHPはバクテリアや哺乳類に対しては変異原性を示さないと言えるようです。しかしながら、酸化ストレスのメカニズムによる直接的間接的にDNAを損傷する可能性や染色体異常を示す証拠が無いわけではありません。また、形態的転換も誘起することが示されてきました。これらのアッセーからの証拠の重みの視点から考察しますと、DEHPについては直接的な遺伝毒性の可能性はありませんが、酸化ストレスの二次的な影響として遺伝毒性への影響が見られる可能性があると言われています。(P301 Toxicological Profile for Di(2-Ethylhexyl)Phthalate (DEHP)2022 ATSDRから)
その他の代表的可塑剤については下の表を参照ください。
| 可塑剤名 | 変異原性試験結果 | 備考(GHS 区分) |
| DOP | 陰性 | 区分に該当しない |
| DBP | 陰性 | 区分に該当しない |
| DINP | 陰性 | 区分に該当しない |
| DIDP | 陰性 | 区分に該当しない |
| DOA | 陰性 | 区分に該当しない |
| DINA | 陰性 | 区分に該当しない |
| TOTM | 陰性 | 区分に該当しない |
| TCP | 陰性 | 区分に該当しない |
代表的な可塑剤の変異原性
内分泌かく乱性とは、生体の内分泌系機能をかく乱させ健康に有害な影響を生ずる毒性をいい、内分泌かく乱性を示す化学物質を「内分泌かく乱化学物質」、「EDCs(Endocrine-Disrupting Chemicals)」と呼びます。内分泌物質である種々のホルモンは生物の体内で作られ血液などに分泌され様々な器官に運ばれて種々の作用を発揮し、役目を終えた後は分解、排出されますが、このEDCsはこの一連の流れに変化を与え、生体に悪影響を及ぼす作用をします。内分泌かく乱性の詳細はJPIAが2017年に発行した「可塑剤インフォメーションNo28」を参照ください1)。
歴史を紐解いてみると、一部のフタル酸エステルが試験管レベルで、ごく弱い女性ホルモン(エストロジェン)様作用を示したとの報告があったことから、環境省(当時は環境庁)が大がかりな調査を行いました。その際、「環境ホルモン戦略計画SPEED’98:内分泌かく乱作用を有すると疑われる化学物質」に多くの可塑剤がリストアップされました。JPIAでは各種可塑剤について試験管レベル及び実際の動物を用いた試験を行い、女性ホルモン様作用を示さないことを確認しました。その後の2003年6月に環境省は9種類の可塑剤について女性ホルモン様作用だけでなく、男性ホルモン様作用や甲状腺ホルモン様作用まで詳細に試験を行い、ヒトにも生態系にも内分泌かく乱作用が認められないとする研究結果を発表しています。
その後、現在に至るまで、欧州を中心に農薬、抗菌剤などの分野で、内分泌かく乱性の検討が進んでおりますが、薬剤以外の一般化学物質については未だ、その定義、判断基準、評価方法が決まっておりません。日本でも環境省がEXTEND2022)にて評価方法等の検討を進めておりますが、欧州と同様の状況です。
また、フタル酸エステルの中で報告例が多いDEHPでは、内分泌かく乱性は「作用」であり、「エンドポイント」は生殖毒性となっていることから、生殖毒性同様に内分泌かく乱性にも「種差」があると考えることができます。
上述のように、一般化学物質の定義・評価方法がないこと、そして「種差」があることから、可塑剤工業会では「フタル酸エステルにヒトへの内分泌かく乱性はない」と考えております。
1)http://www.kasozai.gr.jp/wordpress/wp-content/uploads/2018/12/●KASOZAI_2017_web-1.pdf
2)https://www.env.go.jp/chemi/end/extend2022_00002.html
動物や植物などの生物や水系、海洋、山地、平原等の自然環境は、ある種の循環作用で何らかのバランスができ、生態系を維持しているようです。このバランスは気候変動や地殻内の変動によって自然の力で崩れることもあります。そうすると、それまでの生態系は新たな環境に適用するように変化します。これと同じように、ヒトが地球上で生活を営むことで自然環境が変動することもあります。その要因の一つに、マンメイドの化学物質(例えば工業的に生産される化学物質等)が生態系や自然環境に蓄積することによってそれまでのバランスを損なうこともあり得ます。
バランスを損なっても新たなバランスで生態系や自然環境の営みが健全に維持されれば問題になりませんが、何等かの有害性(adverse effects, toxicity)生じることがあります。マンメイドの化学物質が分解されずに自然環境に蓄積し、生き物の生殖や成長に負の影響をもたらす可能性があります。そして、場合によっては、有害性は生き物にとっては致命的になることもあります。そこで、自然環境で分解しにくく、生態蓄積性のあるそのような有害性の高い物質を規制しようと言う動きが生まれました。それが2001年5月に採択されたストックホルム条約です。
このストックホルム条約は、POPs(Persistent Organic Pollutants、残留性有機汚染物質)条約ともいわます。順次物質が追加され、2023年5月の時点で、PCB等34物質について製造・使用、輸出入が原則禁止になっています。
ストックホルム条約 (残留性有機汚染物質に関するストックホルム条約: Stockholm Convention on Persistent Organic Pollutants (POPs))|外務省 (mofa.go.jp)
各国や地域でも生態蓄積性や難分解性があり有害な物質を規制しようとする動きもあります。EUでは2023年㋃からCMR(発癌性・変異原性・生殖毒性)に加えて、次のようなカテゴリーの有害性も規制の範疇としています。
・人及び環境における内分泌かく乱作用(ED)
・難分解性、高蓄積性、毒性(Persistent, Bioaccumulative, and Toxic)、
・より難分解性、より高蓄積性(very Persistent,very Bioaccumulative)
・難分解性、移動性、毒性(Persistent, Mobile, and Toxic)、
・より難分解性、より移動性(very Persistent, very Mobile)
可塑剤についての生態蓄積性や難分解性ですが、可塑剤は全てがエステル結合を有しております。エステル結合は加水分解によって最終的には元の酸とアルコールに分解します。また、自然環境における水系環境においては、微生物による加水分解を受けることもあります。一例として、自然環境における半減期は、DBP, BBPでは2~3日、DEHP, DINPでは、数週間から数か月と言う報告もあります。
Abiotic degradation of four phthalic acid esters in aqueous phase under natural sunlight irradiation – ScienceDirect ,Ruttapol Lertsirisopon, Satoshi Soda, Kazunari Sei, Michihiko Ike Journal of Environmental Sciences 21(2009) 285–290.
フタル酸エステルは、たとえ環境中に放出されても微生物により容易に分解を受けまた、生体内でも速やかに代謝、排出されるので、蓄積、残留して環境に影響を与えるリスクは極めて低い物質と言えます。
なお、可塑剤工業会で実施したDEHPの環境中での分解挙動は可塑剤工業会のHPにも掲げております。ご参照ください。
フタル酸エステルの分解性について.pdf (kasozai.gr.jp)
化学物質は工場で生産され、工業製品や消費者製品に組み込まれ、使用され、廃棄、リサイクルされます。その行程でその化学物質のほんの一部分が自然環境にも流入し、自然環境(大気、河川、土壌、海水)を移動します。ヒト健康への化学物質の影響と共に、自然界に流入した一部の化学物質が自然環境にどのような影響を及ぼすのか、これが環境影響(動植物への生態影響)です。「ヒト健康への影響」と「環境への影響」との両者に分けてそのリスクに応じて化学物質には別々に規制(制限、禁止)が用意されます。
ここでは、環境影響(動植物への生態影響)の概要をお話ししましょう。自然界に入った化学物質は、最終的には河川や海に運ばれるものと考えられます。従って、河川水や海水、及び河川や海の床にある汚泥に化学物質は溜まる傾向があるようです。このようにして留まった化学物質が環境に存在する動植物にどのような影響が及ぶのかを調査研究するのが、環境影響調査です。動植物の種類も多岐に渡りますし、環境省は水環境に対して「環境での評価管理におけるバイオアッセイ(生物検定法)」を公表(下表参照)しています(2021年9月29日)。汚泥中での調査は極めて困難です。
| No. | 項目 |
|---|---|
| 1 | 化学物質の安全性評価・管理 |
| 2 | 水生生物保全のための環境基準(指針)値設定 |
| 3 | 環境汚染化学物質の簡易・代替測定 |
| 4 | 排水・環境水の評価・管理 |
これはやや抽象的ですが、具体的には、環境省「化学物質の環境リスク初期評価」(1997年~)にありますように、魚類(二次消費者)、甲殻類(一次消費者)、藻類(生産者)の3生物群を用いたバイオアッセイ結果に基づく評価が現在実施されています。
可塑剤工業会では、1993年から海水、河川、及び地下水、及び底質おけるフタル酸エステルの環境モニタリングによる環境濃度調査を、一般財団法人化学物質評価研究機構(CERI)に委託し実施しています。実際に関東地区と関西地区の22か所を定点観測しており、ここ数年の調査結果では、DEHP、DBP、DINPの環境測定濃度はいずれも定量限界値未満でありPNEC(生態系への影響力がないとみなされる環境物質濃度)を下回っていますことから、我々の身近な環境水においてはリスクは低く、これらの可塑剤のリスクは適切に管理されていると考えられています。詳細データに関しましては、可塑剤インフォメーション各号をご参照ください。
このように環境水中で可塑剤がほとんど観測されない理由の一つは、可塑剤のエステル結合が自然環境中で微生物等に分解される、即ち易分解であることにあるとJPIAは考えています。
参考(可塑剤インフォメーションNo.33)
http://www.kasozai.gr.jp/wordpress/wp-content/uploads/2022/01/可塑剤インフォメーションNo.33web.pdf
近年、消費エネルギーを抑えようと省エネが盛んに叫ばれています。住宅環境にもそれが要求されています。一例として挙げれば、冷暖房の効率化です。そのために断熱材の使用が進み、部屋の密閉性も従来よりもはるかに高まっています。結果として室内空気の浄化も不可欠です。室内空気には生活用品や建材等に使用された化学物質が揮発し混入することがあります。このような揮発性の化学物質の中には有害なものもある可能性があります。そこで、世界各国では、室内空気の安全性についての基準を設け、その家に住む人の健康を守るためのガイドラインが設けられてきました。日本もその例外ではありません。
DEHPを例にとってお話ししましょう。DEHPの蒸気圧は極めて低く、常温付近での放散量は問題視する量ではありません。DEHPで可塑化した新建材を施工した室内(壁材や床材全て)の濃度は、28℃下、一年間の連続測定で、当初の数ヶ月間は1μg/m3程度、その後は0.6μg/m3程度でした。厚生労働省の室内濃度指針値は100μg/m3(第23回シックハウス(室内空気汚染)問題に関する検討会(2019))であり、この濃度以下であれば一生涯に渡って室内に暮らしても安全であることが示されています。
因みに、20℃での蒸気圧は3.4×10-5Pa(EUのリスク評価書(2008))ですので、この温度でのDEHPの飽和濃度は5μg/m3程度です。従って、常温付近で室内濃度指針値(100μg/m3)を超えることはあり得ません。
DEHPは加水分解するとフタル酸と原料アルコールに分かれます。実際の消費者製品である床材には、部分的に軟質PVCが用いられています。環境によっては可塑剤が加水分解する可能性もあり、可塑剤の原料アルコール(2-エチル-1-ヘキサノール)の有害性も議論の対象となっています(第22回シックハウス(室内空気汚染)問題に関する検討会(2018))。その後、パブコメなどを経て、議論が継続されており、今後の成り行きが注目されています。
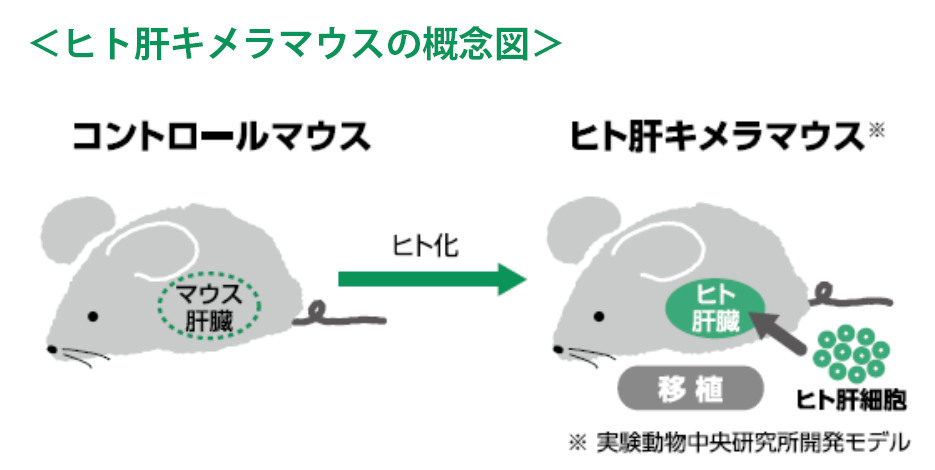 昭和薬科大学の山崎教授らは、マウスの肝臓にヒトの肝臓を移植したキメラマウスを対象にした薬物動態*の実験を行い、実験動物に餌と共に投与されたDEHPが体内でどのような代謝物に変換され,時間と共に投与後どのように体外に排泄されるのかを定量的に観測しました。1) 体の中に吸収されたDEHPはいくつかの代謝物に分解、変性され、その多くが体内で合成された水に溶けやすいグルクロン酸で抱合され、体内に蓄積されることなく投与後ほぼ1 日の内に体外に排泄されました。この報告での一連の実験結果は、ヒトを対象とした倉田らの報告2)と矛盾しません。
昭和薬科大学の山崎教授らは、マウスの肝臓にヒトの肝臓を移植したキメラマウスを対象にした薬物動態*の実験を行い、実験動物に餌と共に投与されたDEHPが体内でどのような代謝物に変換され,時間と共に投与後どのように体外に排泄されるのかを定量的に観測しました。1) 体の中に吸収されたDEHPはいくつかの代謝物に分解、変性され、その多くが体内で合成された水に溶けやすいグルクロン酸で抱合され、体内に蓄積されることなく投与後ほぼ1 日の内に体外に排泄されました。この報告での一連の実験結果は、ヒトを対象とした倉田らの報告2)と矛盾しません。
これらの実験で得られた薬物動態学的パラメータを用いると、ヒト化したPBPKモデル*が構築できます。このモデルとヒト・バイオモニタリング*のデータを用いて、バイオモニタリングの対象となった人たちが一日当たりどれくらいの量のDEHPに量暴露しているのかが算出できます。米国で実施された同齢集団研究、National Health and Nutrition Examination Survey (NHANES) 1999–2010 のヒト・バイオモニタリングデータを用いて得られた、人々の平均的なDEHP暴露量と高暴露となる95%タイルの人々のDEHP暴露量は、それぞれ、0.087(μg /kg 体重/日)、1.3(μg /kg 体重/日)でした。これらの値は、日本の食品安全委員会が2013年に決定した耐容一日摂取量*(30(μg /kg 体重/日))に比べると、桁違いに小さな値であることが分かります。つまり、日常的に暴露しているDEHP からのリスクはほとんどないと言ってよいものと考えられます。環境省が現在実施している日本の大規模同齢集団研究である“エコチル調査*”で収集される検体を用いて、日本での母子のDEHP 暴露量も近々算出できるものと思われます。ご紹介した論文報告の詳細については、原著(参考文献1))をご参照ください。また、可塑剤工業会が発効している「可塑剤インフォメーション(No.28, No.29)」にも、関連記事を紹介しておりますの<ヒト肝キメラマウスの概念図>で、ご覧いただければ幸いです。
| 薬物動態: | 投与された薬物が体内に吸収され、組織に分布し、小腸や肝臓中の酵素により代謝され、排泄される過程を示すもの。 |
|---|---|
| PBPK モデル: | 生理学的薬物動態モデル(Physiologically based pharmacokinetics model)の略。化学物質の血中濃度推移を臓器の血流や容積などの生理学的な情報と代謝速度などの化学物質特有の情報を組み入れて、その体内動態を生理学的な実態に即した形にしたもの。 |
| ヒト・バイオモニタリング: | 化学物質が体に与える影響を尿検査などで個人別に知る方法。同じ年齢集団に対して実施される場合が多い。 |
| 耐容一日摂取量: | ヒトがある物質を一生涯にわたって毎日摂取し続けても健康への悪影響がないと推定される一日当たりの摂取量のこと。通常,物質量〔mg/kg 体重/日〕で示される。 |
| エコチル調査: | 日本中で10万組の子どもたちとその両親が参加している大規模な疫学調査「子どもの健康と環境に関する全国調査」。環境省が 2011年より実施している。 |
参考文献
1) “Human biofluid concentrations of mono(2-ethylhexyl)phthalate extrapolated from pharmacokinetics in chimeric mice withhumanized liver administered with di(2-ethylhexyl)phthalate and physiologically based pharmacokinetic modeling” Adachi K.,Suemizu H., Murayama N., Shimizu M., Yamazaki H.,Environmental Toxicology and Pharmacology, 39, 1067–1073, 2015.
2) “Metabolite profiling and identification in human urine after single oral administration of DEHP” Kurata Y., Shimamura N., KatohM.,The Journal of Toxicological Sciences,37, 401-414, 2012